Autor/en: Wohlgemuth, Walter A. | Dießel, Linda | Kisser, Ulrich
Autor/en: Wohlgemuth, Walter A. | Dießel, Linda | Kisser, Ulrich
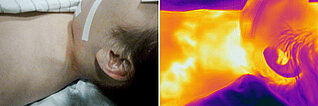
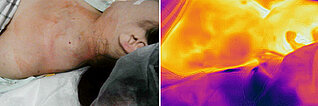
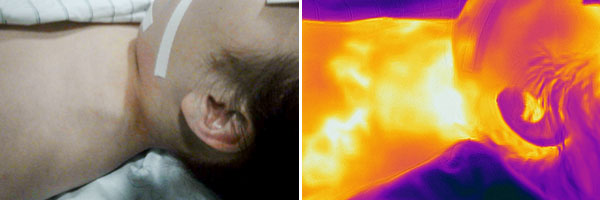
12-jährige Patientin, vor 3 Jahren erstmals sichtbare, progrediente Schwellung supraklavikulär links; Zustand nach bisher insgesamt 7 Embolisationen mit nBCA-Kleber, EVOH und reinem Ethanol. Nach einer Embolisation mit Ethanol Entwicklung einer Nekrose, Abheilung über 6 Monate. Trotz dieser Therapie weitere schnelle Proliferation, lokale Schmerzen. Die Infrarotthermographie im Bereich der pulsatil tastbaren Schwellung zeigt eine deutliche Überwärmung (hell bis weiß im Bild rechts) sowie eine oberflächliche, erwärmte Drainagevene.
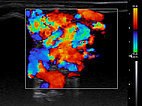
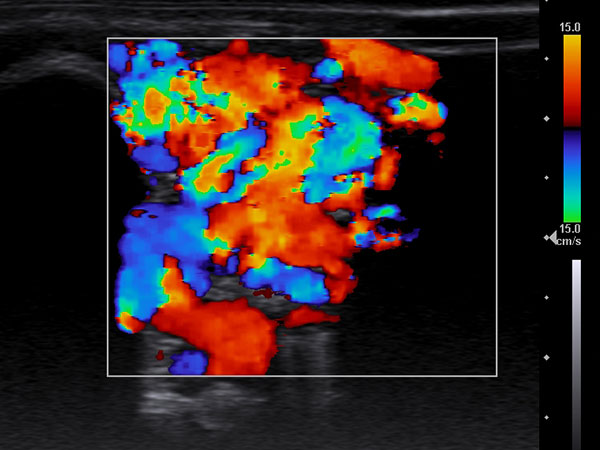
In der farbkodierten Duplexsonographie (FDKS) sieht man bereits bei einem mittleren Setting der Pulswiederholungsfrequenz eine massive Perfusion praktisch der gesamten, aus durchströmten Gefäßen bestehenden Läsion. Dies typisch für eine Fast-flow-Malformation, hier eine arteriovenöse Malformation.
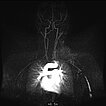
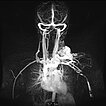
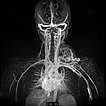
Dynamische, kontrastmittelunterstützte, zeitlich hochaufgelöste MR-Angiographie; Darstellung 46 s nach intravenöser Kontrastmittelapplikation. Das Kontrastmittel hier noch vorwiegend im kleinen Kreislauf der Lunge (Frühphase).
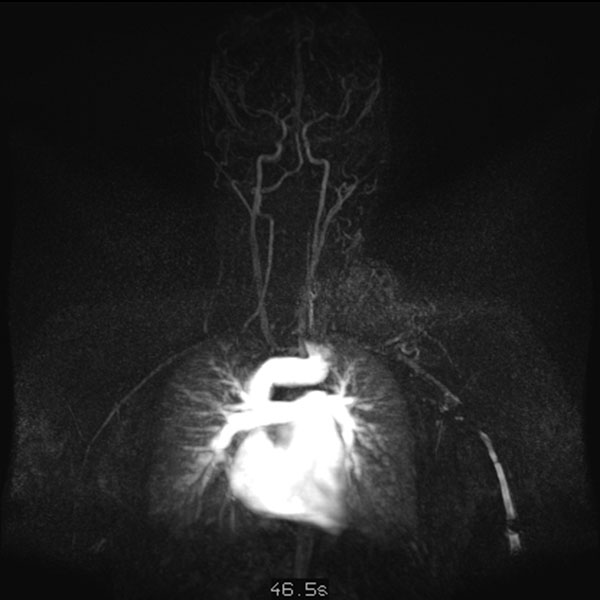
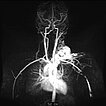
Dynamische, kontrastmittelunterstützte, zeitlich hochaufgelöste MR-Angiographie; Darstellung 52 s nach intravenöser Kontrastmittelapplikation. Bereits 5 s später fließt das Kontrastmittel sofort durch die arteriovenöse Malformation hindurch, eine Drainagevene ist ebenfalls bereits direkt kontrastiert. Typischer, extrem schneller Durchfluss einer arteriovenösen Malformation als Fast-flow-Läsion.
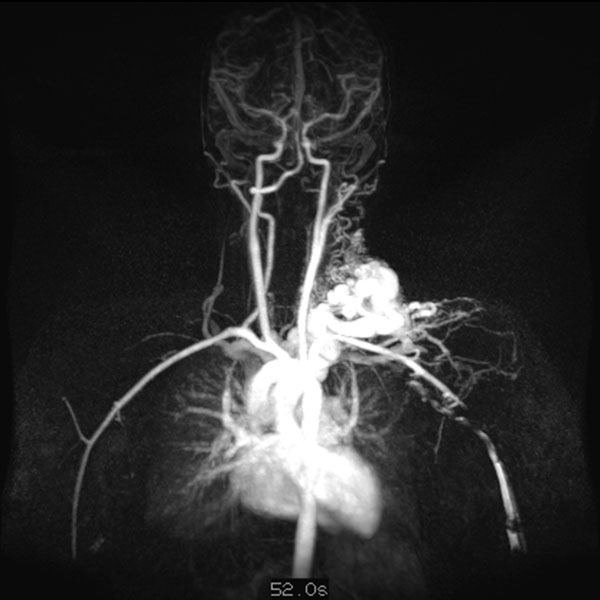
Dynamische, kontrastmittelunterstützte, zeitlich hochaufgelöste MR-Angiographie; Darstellung 57 s nach intravenöser Kontrastmittelapplikation. Weitere 5 s später nochmals bessere Darstellung des venösen Abstroms aus der arteriovenösen Malformation.
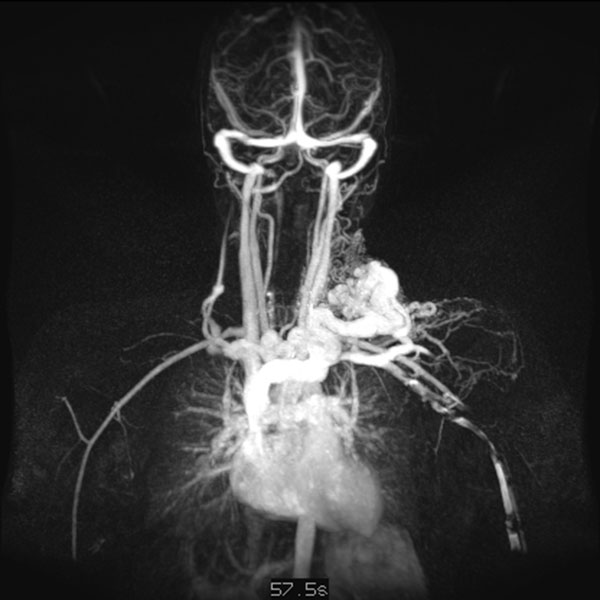
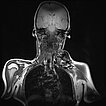
In der nativen, T1-gewichteten, koronaren MRT zeigt sich die arteriovenöse Malformation als stark hypointense Raumforderung ohne eigentlich soliden Charakter. Das fehlende MRT-Signal ist durch den schnellen und starken Durchfluss bedingt (sogenannte „Flow-voids“). Das Blut strömt hier so schnell durch die Läsion, dass es kein signalgebendes Echo erzeugen kann.
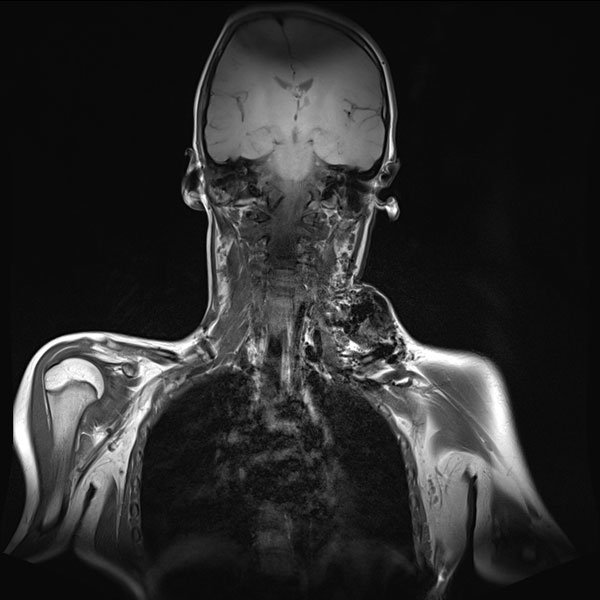
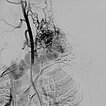
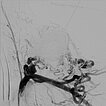
In der digitalen Subtraktionsangiographie (DSA) nach Injektion in die linke A. carotis communis stellen sich multiple, kaum zählbare zuführende arterielle Feeder dar, die den Nidus der arteriovenösen Malformation speisen. Sofortiger und direkter venöser Abstrom aus der Läsion.
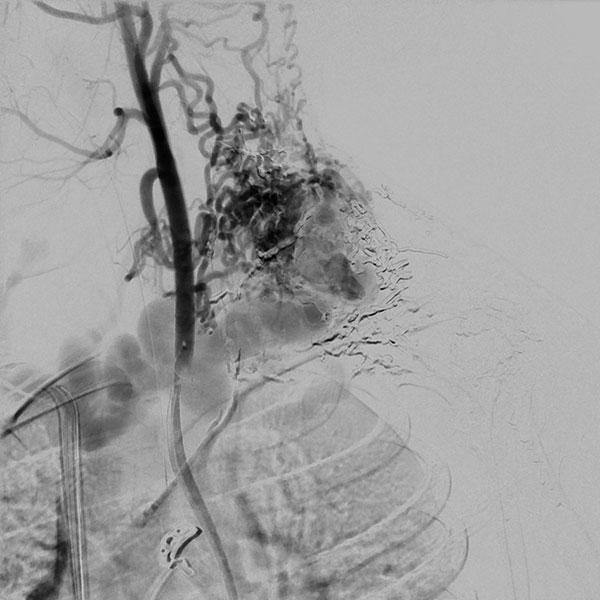
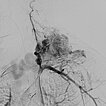
Digitale Subtraktionsangiographie (DSA) nach Injektion in die linke A. subklavia. Es stellen sich ebenfalls unzählige zuführende arterielle Feeder dar, direkt aus der A. subklavia, aber auch multiple Zuflüsse direkt aus der linken A. vertebralis. Aufgrund der multiplen, feinen, kaum einzeln identifizierbaren arteriellen Zuflüsse ist eine rein transarterielle Embolisation technisch nicht möglich und auch nicht zielführend.
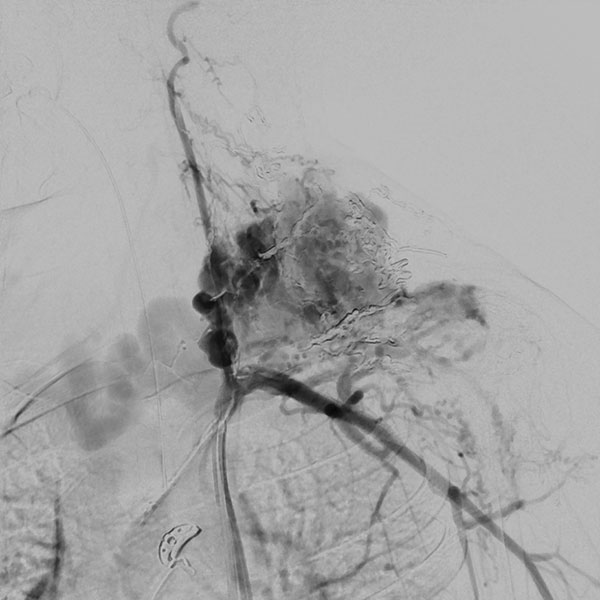
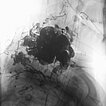
Digitale Subtraktionsangiographie (DSA), Nativbild. Der Nidus der arteriovenösen Malformation wurde jetzt in 2 Sitzungen sukzessive nach direkter Punktion mit einer Nadel mit dem flüssigen, zäh wie Lava fließenden Embolisat Ethylen-Vinyl-Alkohol-Kopolymer (EVOH) aufgefüllt im Sinne einer Embolisation. Der Nidus ist am Ende nach Injektion von 37 Ampullen des röntgendichten Embolisats komplett aufgefüllt. Es kommt zu keinem Durchstrom mehr, die arteriovenöse Malformation ist verschlossen.
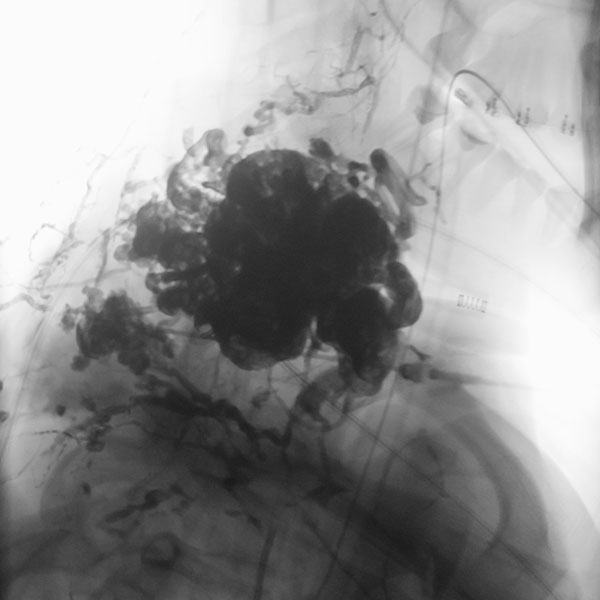
Digitale Subtraktionsangiographie (DSA) mit proximaler Injektion in die linke A. subklavia mit Darstellung der A. vertebralis nach Abschluss der 2. Embolisation. In dieser späten Phase nach Injektion stellen sich zwar noch einige arterielle Feeder dar, diese finden jedoch keinen Anschluss mehr an den Nidus der arteriovenösen Malformation. Auch zeigt sich kein venöser Abstrom mehr. Damit ist die AVM verschlossen.
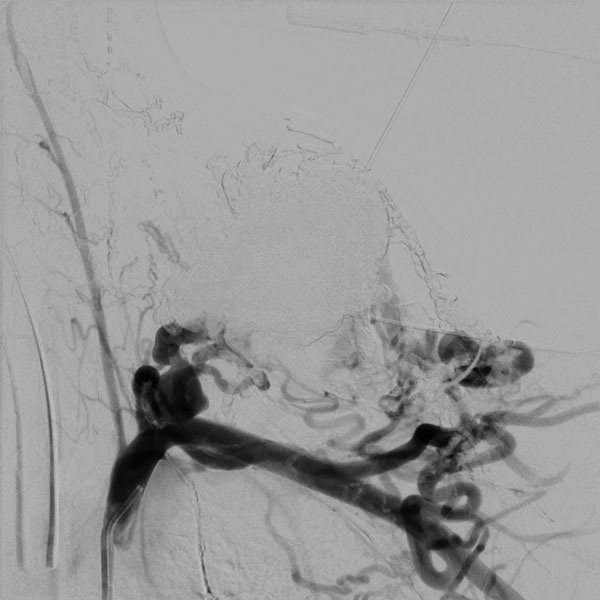
Die Infrarotthermographie nach Ende der 2. Embolisation zeigt ebenfalls eindrucksvoll, dass die Schwellung durch die arteriovenöse Malformation zwar noch vorhanden ist, die Überwärmung jetzt jedoch nicht mehr besteht. Lokal ist die Temperatur unmittelbar nach der Embolisation sogar etwas kühler.
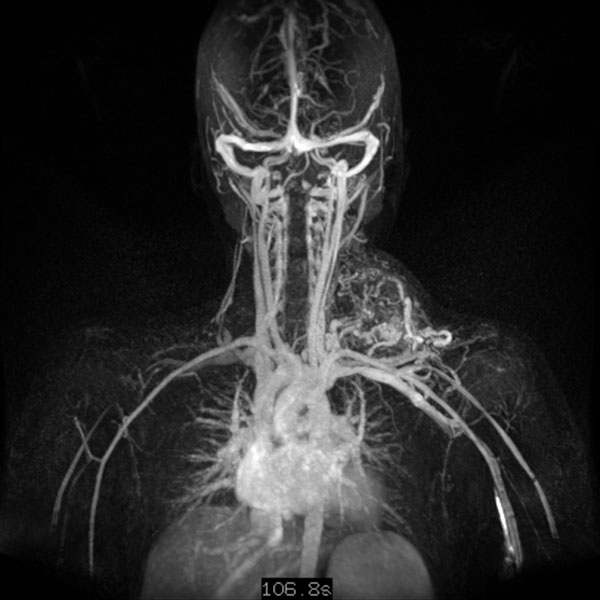
Dynamische, kontrastmittelunterstützte, zeitlich hochaufgelöste MR-Angiographie 5 Tage nach Embolisation; Darstellung in der Spätphase 107 s nach intravenöser Kontrastmittelapplikation. Auch nach diesem langen Delay zeigt sich keine Restperfusion der arteriovenösen Malformation mehr. Lediglich einige nicht verschlossene arterielle Zuflüsse sind noch dargestellt, diese finden jedoch keinen Abstrom oder Anschluss an die AVM mehr.
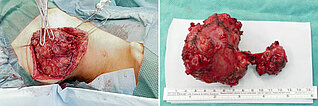
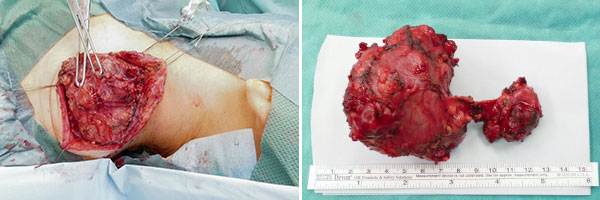
Durch den vollständigen Verschluss ist die arteriovenöse Malformation jetzt erstmals im Prinzip operabel. Um die lokale Raumforderung zu entfernen und auch um sicherzustellen, dass es nicht im langjährigen Verlauf doch noch eventuell zu einem Rezidiv kommt, wird die AVM mikrochirurgisch präpariert und schließlich in einer Sitzung vollständig und komplikationslos reseziert. Auf dem Präparat optisch gut sichtbar der Ausguss („Cast“) der Gefäße des Nidus durch das schwarze Embolisat.
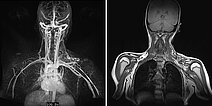
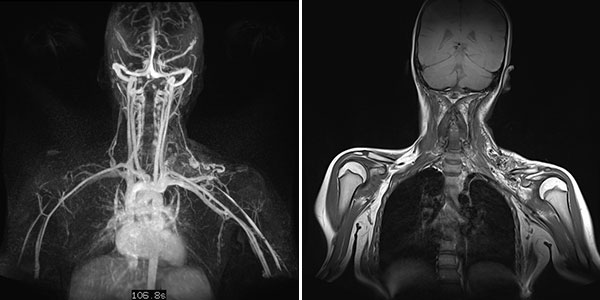
Dynamische, kontrastmittelunterstützte, zeitlich hochaufgelöste MR-Angiographie (linkes Bild) 5 Tage nach offener Resektion des verschlossenen Nidus; Darstellung wiederum in der Spätphase 107 s nach intravenöser Kontrastmittelapplikation. Auch nach diesem langen Delay zeigt sich keine Restperfusion der arteriovenösen Malformation mehr. Der initial in der koronaren, T1-gewichteten, nativen MRT (rechtes Bild) vormalig noch sichtbare Raumforderungseffekt der AVM ist nach der Resektion verschwunden.
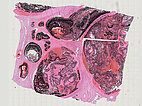
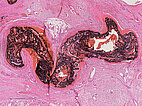
Histopathologischer Schnitt des Resektionspräparates; Hämatoxylin-Eosin-Färbung, 5-fache Vergrößerung (Übersicht): Es finden sich multiple, vermehrte Gefäße der AVM, vorwiegend arteriell oder arterialisiert mit dicker Gefäßwandung. Diese sind bis auf die kapilläre Ebene ausgefüllt mit dem schwarzen Embolisat (Ethylen-Vinyl-Alkohol-Kopolymer; EVOH).
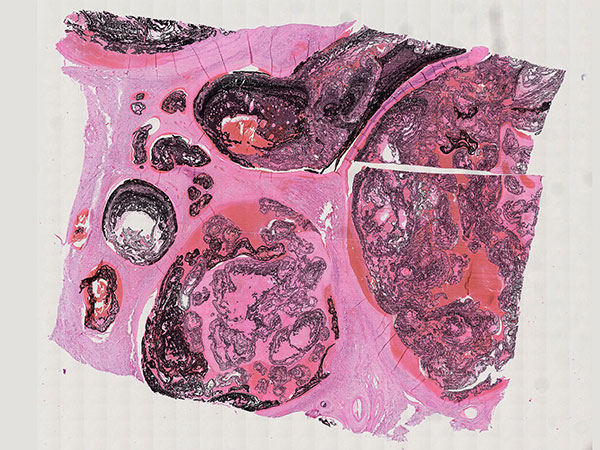
Histopathologischer Schnitt des Resektionspräparates; Hämatoxylin-Eosin Färbung, 15-fache Vergrößerung: Innerhalb der multiplen dilatierten, netzartigen Gefäßlumina der arteriovenösen Malformation finden sich auch alte Thromben, zum Teil organisiert als Fibrin. Die dazwischen liegenden, perfundierten Anteile sind komplett mit dem schwarzen Embolisat EVOH ausgefüllt.
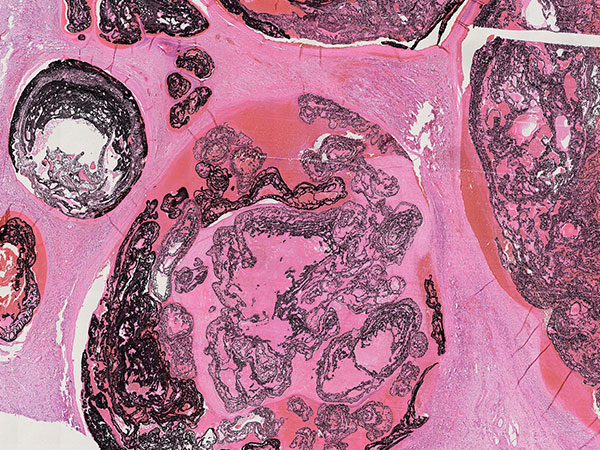
Histopathologischer Schnitt des Resektionspräparates; Hämatoxylin-Eosin Färbung, 30-fache Vergrößerung: Zuführende Feeder-Arteriole mit dicker Gefäßwandung sind vollständig mit dem Embolisat gefüllt.
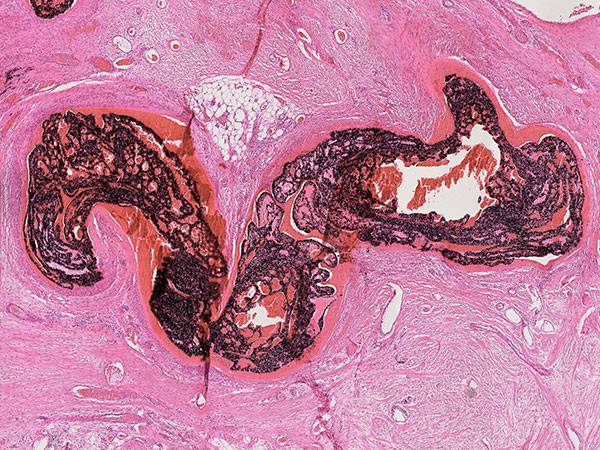
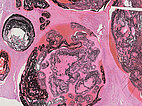
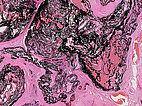
Histopathologischer Schnitt des Resektionspräparates; Hämatoxylin-Eosin Färbung, 14-fache Vergrößerung: Auf der Ebene des Nidus mit seinen multiplen, direkten arteriovenösen Kurzschlüssen ist in den bizzaren, fuchsbauartigen dysplastischen Gefäßräumen nicht mehr eindeutig zwischen arteriellen, kapillären und venösen Gefäßstrukturen zu unterscheiden. Auch diese Räume sind von dem schwarzen Embolisat gefüllt, das unter Druck („plug & push Technik“) in den Nidus eingepresst wurde.
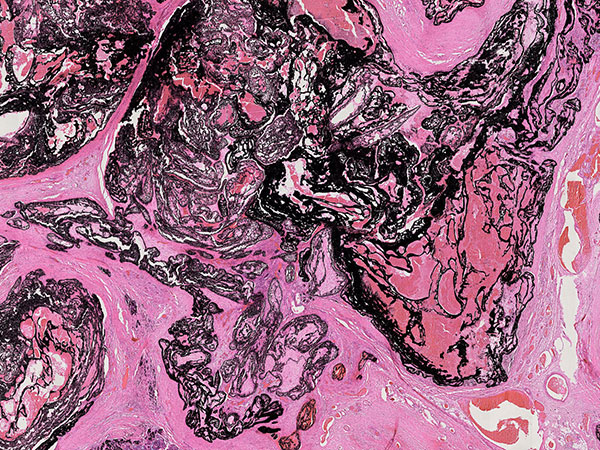
Arteriovenöse Malformationen sind insbesondere dann schwer zu behandeln, wenn es zu einem Rezidiv gekommen ist und die Läsion bereits mehrfach voroperiert ist und dann proliferiert. In einer solchen Situation ist eine möglichst komplette, kombinierte Embolisation bis zum vollständigen Verschluss und danach, wenn technisch irgend möglich, eine komplette Resektion des verschlossenen Nidus anzustreben.
Die Therapiesteuerung erfolgte auch bei dieser Patientin interdisziplinär mit HNO, Radiologie, Kinderkardiologie und Pathologie.
Es gelang mit einer hohen Dosis des Embolisates in 2 Sitzungen die arteriovenöse Malformation zu verschließen. Auch die anschließende Resektionsoperation erfolgte dann vollständig und ohne Komplikationen.
Die durchgeführte Histopathologie des Resektates zeigt schön die Feinstruktur der Gefäßarchitektur einer arteriovenösen Malformation. Anders als die Slow-flow-Malformationen (venöse oder lymphatische Malformation) steht die arteriovenöse Malformation als Fast-flow-Läsion durch die unmittelbaren arteriovenösen Shunts unter hohem, ständigen Durchfluss und damit auch unter hohem Druck. Damit arterialisiert auch der venöse Abstrom schnell, die Gefäßwände werden dicker. Es ist kaum zu unterschieden, ob es sich bei den vielen kleinen, großteils dysplastischen Gefäßanschnitten um Arteriolen oder Venolen handelt. Alle zeigen reaktiv einen deutlich wanddicken, arterialisierten Gefäßwandaufbau. Gut zu sehen ist in diesem Fall im Feinschnitt auch das bis auf kapilläre Ebene reichende Embolisat, das den Nidus verschließt.
Insgesamt ist die Entstehung eines weiteren Rezidivs bei dieser Patientin jetzt unwahrscheinlich. Dennoch ist auch diese Patientin in einem Nachsorgeprogramm.
Publiziert: 2022
Alle Abbildungen © Wohlgemuth/Dießel/Kisser